Ein Expertisebereich der Fachgruppe DezE
Bitte die Logos anklicken, für weitere Informationen
Brennstoffzellentechnik und Elektrolyse
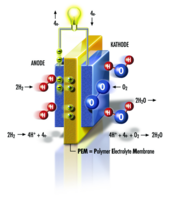
Wasserstoff-Brennstoffzelle
Ausführliche Beschreibung anzeigen
Die Grafik zeigt den Querschnitt einer einzelnen Brennstoffzelle vor einem hellgrauen Hintergrund. Der Aufbau gliedert sich von links nach rechts in drei Hauptbereiche: Anode (Minuspol), Elektrolyt-Membran und Kathode (Pluspol).
- Linke Seite (Anode):
Zwei Wasserstoff-Moleküle (2H₂) treffen auf die Anode. Der Wasserstoff wird aufgespalten. Die Reaktionsgleichung lautet: 2H₂ → 4H⁺ + 4e⁻. Es entstehen vier positiv geladene Wasserstoff-Ionen (Protonen) und vier negativ geladene Elektronen. - Mitte (Membran):
Eine gelbe Trennschicht befindet sich zwischen Anode und Kathode. Sie ist beschriftet mit „PEM = Polymer Electrolyte Membrane“. Diese Membran ist nur für die positiven Protonen (H⁺) durchlässig, die von links nach rechts wandern. - Äußerer Stromkreis:
Die Elektronen (4e⁻) können die Membran nicht passieren. Sie fließen über einen externen Leiter von der Anode oben über eine leuchtende Glühbirne zur Kathode. Dies symbolisiert den Stromfluss. - Rechte Seite (Kathode):
Ein Sauerstoff-Molekül (O₂) trifft auf die Kathode. Die Elektronen aus dem Stromkreis, die Protonen durch die Membran und der Sauerstoff treffen zusammen. Sie reagieren zu zwei Wasser-Molekülen (2H₂O). Die Reaktionsgleichung lautet: 4H⁺ + 4e⁻ + O₂ → 2H₂O.
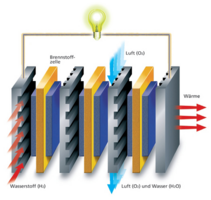
Brennstoffzellen-Stack
h-tec-education.com
Ausführliche Beschreibung anzeigen
Die Grafik zeigt einen sogenannten „Stack“ (Stapel), bei dem mehrere flache Brennstoffzellen wie in einem Sandwich hintereinander angeordnet sind.
- Aufbau:
Der Stapel besteht abwechselnd aus grauen Platten (Bipolarplatten mit Kanälen) und den eigentlichen elektrochemischen Zellen (gelb/orange und blau dargestellt). Ein goldener Bügel verbindet die erste und die letzte Platte des Stapels elektrisch mit einer leuchtenden Glühbirne, was die Energieerzeugung demonstriert. - Stoffströme:
Rote Pfeile an der linken Seite zeigen, dass Wasserstoff (H₂) in die Zwischenräume der Platten eingeleitet wird.
Hellblaue Pfeile von oben zeigen, dass Luft (O₂) in den Stapel strömt.
Dunklere blaue Pfeile treten unten aus und symbolisieren das „Abgas“: Luft (O₂) und Wasser (H₂O).
Drei rote Pfeile auf der rechten Seite zeigen aus dem Stapel heraus und sind mit „Wärme“ beschriftet, was die Abwärme als Nebenprodukt der Reaktion verdeutlicht.
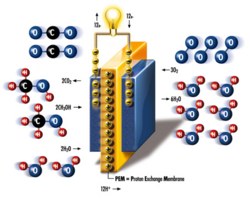
Methanol-Brennstoffzelle
Ausführliche Beschreibung anzeigen
Diese Grafik zeigt den Querschnitt einer Direktmethanolbrennstoffzelle. Der Aufbau (Anode, Membran, Kathode) ähnelt der Wasserstoff-Brennstoffzelle, nutzt aber Methanol als Brennstoff.
- Linke Seite (Anode):
Zwei Methanol-Moleküle (2CH₃OH) und zwei Wasser-Moleküle (2H₂O) reagieren an der Anode. Dabei wird Kohlendioxid (2CO₂) freigesetzt. Es werden 12 Elektronen (12e⁻) freigesetzt, die über den externen Stromkreis (mit Glühbirne) fließen. Gleichzeitig wandern 12 Protonen (12H⁺) durch die gelbe Membran. - Mitte (Membran):
Die gelbe Membran in der Mitte ist beschriftet mit „PEM = Proton Exchange Membrane“. Sie lässt die positiv geladenen Teilchen zur anderen Seite durch. - Rechte Seite (Kathode):
Drei Sauerstoff-Moleküle (3O₂) treffen auf die Kathode. Der Sauerstoff reagiert mit den 12 Elektronen und den 12 Protonen. Es entstehen sechs Wasser-Moleküle (6H₂O), die nach rechts abgeführt werden.
Für die dezentrale Energieversorgung ist der Einsatz von Elektrolyseuren, Wasserstoffspeichern und Brennstoffzellen unumgänglich, da Batteriespeicher zwar den Tagesgang von Wind- und Sonnenenergie ausgleichen können, für den Ausgleich von jahreszeitlichen Schwankungen aber zu groß, schwer und teuer wären. Kombinierter Einsatz von Wind- und Sonnenenergie kann hier einen gewissen Ausgleich schaffen, da PV-Anlagen im Sommer mehr Strom liefern, Windkraftanlagen in den anderen Jahreszeiten, aber nicht für alle Versorgungsszenarien sind beide Energieformen einsetzbar.
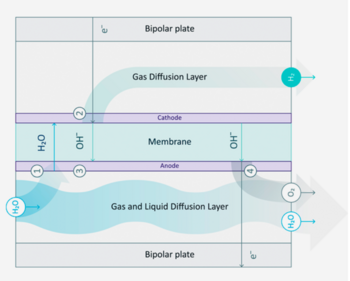
Funktion eines AEM Elektrolyseurs
Quelle: Enapter
Ausführliche Beschreibung anzeigen
Die Grafik zeigt den vertikalen Aufbau einer Elektrolysezelle. Es handelt sich um eine AEM-Elektrolyse (Anion Exchange Membrane), erkennbar am Transport von Hydroxid-Ionen (OH⁻). Der Aufbau ist in horizontalen Schichten dargestellt, die von oben nach unten wie folgt beschriftet sind:
- Bipolar plate (Bipolarplatte, oben)
- Gas Diffusion Layer (Gas-Diffusionsschicht)
- Cathode (Kathode – lila Linie)
- Membrane (Membran – hellblauer Bereich in der Mitte)
- Anode (lila Linie)
- Gas and Liquid Diffusion Layer (Gas- und Flüssigkeits-Diffusionsschicht)
- Bipolar plate (Bipolarplatte, unten)
Die chemischen Prozesse und Stoffströme sind durch Pfeile markiert:
- Wasser (H₂O): Tritt unten links in die „Gas and Liquid Diffusion Layer“ ein. Ein Pfeil zeigt, dass Wasser von dort nach oben durch die Anode und die Membran zur Kathode diffundiert.
- Elektronen (e⁻): Ein Pfeil zeigt von oben durch die Bipolarplatte hinab zur Kathode (Stromzufuhr). Ein weiterer Pfeil zeigt von der Anode unten durch die untere Bipolarplatte hinaus (Stromabfuhr).
- Reaktion an der Kathode (oben): Hier entsteht Wasserstoff. Ein Pfeil mit der Beschriftung H₂ zeigt nach rechts aus der „Gas Diffusion Layer“ heraus.
- Transport durch die Membran: Hydroxid-Ionen (OH⁻) wandern von der Kathode oben durch die Membran nach unten zur Anode.
- Reaktion an der Anode (unten): Hier reagieren die OH⁻-Ionen. Sauerstoff entsteht und wird nach rechts ausgeleitet (Pfeil mit O₂). Zudem wird überschüssiges Wasser (H₂O) unten rechts ausgeleitet.
Hier kommen Elektrolyseure zur Gewinnung von Wasserstoff aus überschüssigem Strom ins Spiel, und Brennstoffzellen zur Rückverstromung des gespeicherten Wasserstoffs. Elektrolyseure sind zentrale Komponenten in der Wasserstoffproduktion, insbesondere im Kontext der nachhaltigen Energieerzeugung und -speicherung. Sie ermöglichen die elektrochemische Spaltung von Wasser in Wasserstoff und Sauerstoff mittels elektrischer Energie. Insbesondere im großen Maßstab lässt sich Wasserstoff sehr günstig in Salzkavernen speichern, eine bei Erdgas seit langem erprobte Technologie. Für den Einsatz in Häusern, Industriebetrieben und Quartieren bieten sich Druckgasspeicher mit bis zu 45 bar oder Stahlflaschenbündel mit bis zu 300 bar an. Wir prüfen auch den Einsatz von Metallhydridspeichern, die das geringste Volumen aller Wasserstoffspeicher in Anspruch nehmen, sogar nur etwa die Hälfte von flüssigem Wasserstoff, der wegen seiner niedrigen Siedetemperatur von -253 Grad Celsius schwer handhabbar ist und hohen Aufwand zur Verflüssigung braucht. Diese Technologie gewinnt zunehmend an Bedeutung, da Wasserstoff als sauberer Energieträger betrachtet wird, der fossile Brennstoffe ersetzen kann und dabei keine klimaschädlichen CO₂-Emissionen verursacht. Elektrolyseure spielen eine Schlüsselrolle in der Entwicklung von Wasserstoffwirtschaften, da sie eine direkte Nutzung von erneuerbaren Energiequellen ermöglichen und zur Dekarbonisierung verschiedener Sektoren wie Industrie, Mobilität, öffentlichen Einrichtungen und Privathaushalten beitragen können.
Vor allem im industriellen Bereich ist auch der Einsatz von Methanolbrennstoffzellen denkbar, dann allerdings eher als Ersatz für herkömmliche, mit Diesel oder Erdgas betriebene Notstromaggregate bzw. Kraft-Wärme-Kopplung-Anlagen. Bei diesen Brennstoffzellen werden Methane und andere Kohlenwasserstoffe direkt in Wasserstoff umgewandelt. Dies wird auch als interne Reformierung bezeichnet, es ist also keine externe Quelle erforderlich, die Wasserstoff erst aus natürlichen Gasen wie Erdgas oder Biogas gewinnt. Methanol ist preiswert und als flüssiger Kraftstoff leicht zu lagern. Wird im Zuge der Sektorenkopplung die entstandene Abwärme genutzt, lassen sich Wirkungsgrade bis hin zu 85% erreichen.